https://www.nature.com/articles/nrg.2016.87
Abstract
동시에 발생하는 질병들(co-occurrence of disease)을 통해 다기능적인 유전자 및 경로의 네트워크를 설명한다.
Introduction
background를 정리하고, 논문의 주장을 요약합니다.
BACKGROUND : comorbidities 연구와 network biology
1. 최근 분자 수준의 시스템 생물학 및 역학 분야에서 두 가지 이상의 질병을 앓고 있는 환자의 질병 진행 패턴에 대한 관심이 높아지고 있습니다.
2. 모든 생물학적 시스템은 본질적으로 동적(=유동적이다, dynamic)이며, pleiotropy, robustness, rewiring 과 같은 동적인 특징을 갖는다. 유전자 유전자좌뿐만 아니라 단백질과 경로도 상황과 시간에 따라 여러 가지 역할(=Multifunctionalities)을 할 수 있다. 이런 다기능성은 pleiotropy에 관여하여 comorbidities을 초래할 수 있다.
- pleiotropy : 하나 이상의 형질에 영향을 미치는 genetic locus의 특징
- robustness : 외부 혹은 내부 교란(conditional changes)으로부터 기능을 유지할 수 있는 능력
- rewiring : 조건부 변화에 따른 생물학적 요인들간의 상호작용의 재구성
- Comorbidities : 한 개체에서 두 가지 질병 상태가 공존하는 상태
3. network biology 가 complex disease(ex. comorbidites)를 합리화(rationalizing, 이해하기 쉽게 설명하다)하는데 선호되는 모델이다. 또한, 시간과 상황에 따라 변화하는 생물학적 요소(dynamic 특성)을 잘 반영한다.
PREVIOUS WORK : dynamic feature를 고려한 분석의 강조
1. 전통적인 네트워크에는 genetic interaction netwokrs 와 physical interaction networks가 있으며, 단일 조건에서 생성된 '정적'(static)인 네트워크이다. dynamic disease states에 대한 통찰을 제공하지 못한다.
-> 왜 dynamic diseaset states 일까? : 내부 조절 반응과 환경 간섭 및 치료에 의한)
2. 오믹스' 기술(예: 단일 세포 기술)의 발전으로 이제 동적 질병 패턴에 대한 보다 심층적인 특성 분석이 가능해졌다.(예: 차등 네트워크)
- Differential networks (차등 네트워크)
- 상황에 따른(context-specific) 상호작용을 나타냄 : 해당 상황에 따라 활성화되거나 억제되는 유전자간의 상호작용 분석 가능
- 시스템의 비특이적이지만 지배적인 상호작용(예: 하우스키핑)을 걸러낼 수 있습니다
- quantitative techniques (예: such as time‐ and stimuli‐resolved mass spectrometry)
- EGF를 자극하여 HEK293T 세포에서 허브 단백질 GRB2의 rewiring 관찰하여 EGF가 GRB2 복합체 형성에 중요한 역할을 하는 것을 확인함
3. 한 개인에게 동시에 발생하는 질병의 맥락에서 다발성, 견고성, 재배선과 같은 동적 네트워크 개념을 고려하는 것이 중요하다
- Rewiring-based analysis가 암을 유발하는 주요 변이(gene driver mutations)의 식별 가능성을 높일 수 있다.
(rewrie signaling netowrk 분석을 통해 해당 암 변이가 6가지 매커니즘을 통한다는 것을 분류할 수 있었다) 19 - 144개의 서로 다른 인간 조직과 세포 유형에 대한 포괄적인 조직별 기능적 상호 작용 네트워크 라이브러리를 개발 12
CHALLENGES : dynamic feature를 고려한 분석의 강조
복잡한 질병에 이러한 동적 개념을 적용하는 것에 어려움을 겪어왔다.
1.기술적 제약
2. 일관되지 않은 용어사용
복잡한 질병에서 특히 해당 어려움이 심화되는데,
*예를 들어, 암과 패혈증을 동시에 앓고 있는 환자의 경우, 더 급성인 상태인 패혈증의 존재에 따라 암 치료가 조절되어야하며, 다약제 사용(여러 가지 약물을 동시에 사용하는 것)에 따른 치료 효과를 감소 및 예상치 못한 부작용에 대해 대비해야되기 때문이다.
The concept of comorbidity.
comorbidity란 한 개인 내에서 주요 질병 외에 하나 이상의 추가적인 질병이 존재하는 상황
정신 질환에서 동반 질환 진단이 높은 비율로 오류로 인한 것일 수 있다는 비판 존재.
동반 질환들이 어떻게 서로 인과적 관련이 있는지에 대한 명확성 부족.
동반 질환과 다발성 질환(multimorbidity) 용어는 종종 서로 바꿔 사용.
둘다 유전적요인과 환경적 요인을 질병의 원인으로 보고 있다.
*comorbidity : 주 질병을 중심으로 치료
예를 들어, 환자가 심장 질환을 주 질병으로 가지고 있고, 동시에 당뇨병과 고혈압을 가지고 있다면, 이 추가적인 질병들은 동반 질환으로 분류.
* multimorbidity : 환자 중심적인 관점에서 질병을 고려하며, 어떤 질병도 우선 순위에 두지 않는다.
예를들어, 위 환자에 대해 심장 질환, 당뇨병, 고혈압 사이에 특정한 '주요 질병'을 설정하지 않음.
해당 논문에서는 위 정의(임상 정의)를 이용
*역동반 질환(inverse comorbidity) : 같은 개인에서 특정 질병들이 함께 나타날 확률이 낮은 현상
*오프타겟 효과(off-target effect) : 의약품이나 치료제가 의도한 대상 이외의 다른 대상에 작용하여 예상치 못한 부작용이나 효과를 발생시키는 현상
예: 오프타겟 효과로 제2형 당뇨병 환자에서 메트포르민이라는 항당뇨병 약물을 사용할 경우 일부 암의 발병 위험이 감소
-> 이 개념을 통해 환자의 적절한 치료 접근 방법을 선택할 수 있습니다.
Multimorbidity space
많은 환자들은 다양한 심각도에서 여러 진단과 인지되지 않은 상태를 동시에 가지고 있다.
환자의 상태를 다중 질병 공간에서 한 점으로 볼 수 있으며, 각 차원은 표현형에 해당된다.
증상, 진단, 유전학 및 분자 프로필과 같은 환자의 표현형의 미세한 특징들을 기준으로 환자들을 더 포괄적으로 분류함으로써,
다중 질병 공간에서 각 환자의 보다 정확한 위치를 찾을 수 있습니다.
-> 최근 연구에는 이러한 표현을 단순화하고 계층적 관계 및 의존성을 포착하기위해 딥러닝을 사용함 51
*깊은 표현형 분석은 다중 질병 공간의 차원 수를 증가시키는 비용이 들지만, 희귀 변이를 탐지하는 데 필요한 코호트 크기를 줄일 수 있다.
환자들은 평생 동안 새로운 진단을 받거나 다른 질병에 대한 치료를 받으면서 다중 질병 공간에서 궤적을 따라 움직인다.
*환경적 및/또는 유전적 변이에 의해 궤적을 달리하는데, 해당 전환이 해로울수도 보호적일 수도 있다.
Pleiotropy and multifunctionality
많은 질병들이 유전적 구조를 공유하고 있음이 밝혀짐
예: 면역 매개 질병에서 공유된 질병 위험 변이와 경로의 두드러진 중복이 관찰되어, 광범위한 다형성 효과가 있음을 시사
여전하 다형성이 유전자와 표현형 사이에 어떻게 작용하는지 구체적인 생물학적 경로를 완전히 이해하지 못했다(블랙 박스).
그리고 특히 여러 질병이 동시에 나타나는 상황에서 어떤 역할을 하는지 확립되지 않았다.
Five models of pleiotropy and multifunctionality.
*다형성의 여러 정의를 설명하고 복잡한 질병의 공존 질환 및 동적 네트워크와의 관계에 대해 논의
지난 20년간의 리뷰는 분자적 맥락에서 일관되게 다형성을 정의하려고 시도했지만, 아직 명확한 합의에 도달하지 못했다.
유전자 기능수 관점, 기본 메커니즘과 관련된 관점, GWAS 관점 등 다양.
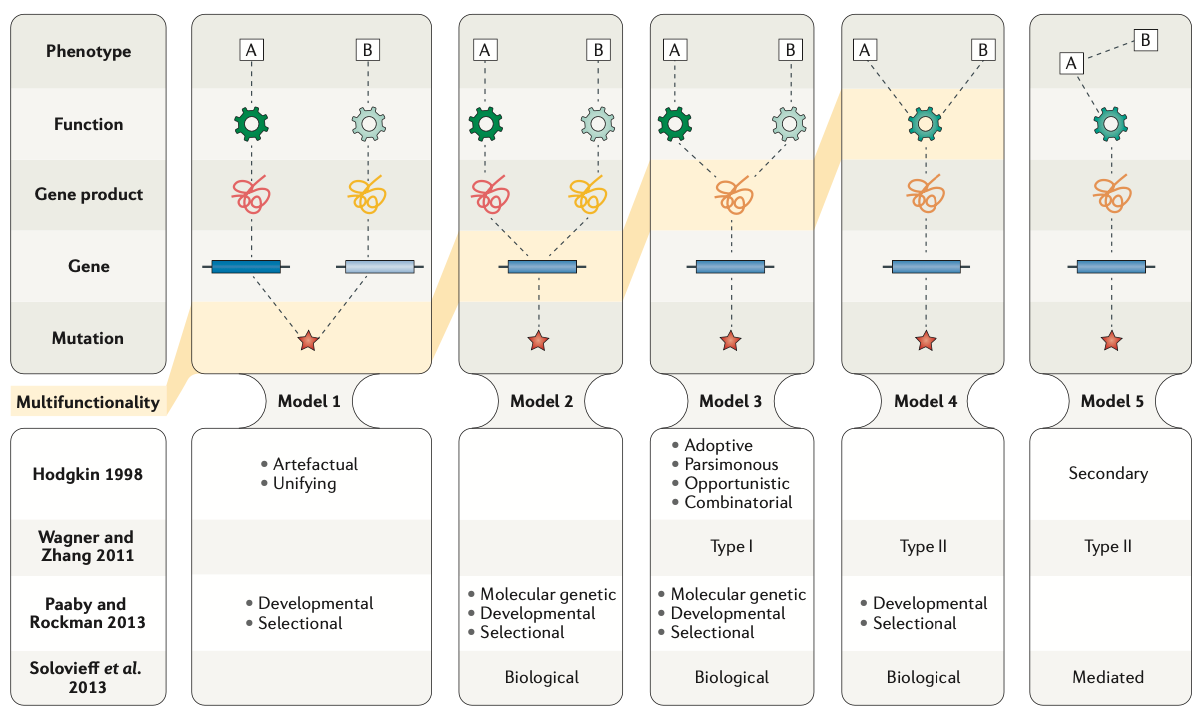
본 논문에서는 통합적 관점의 pleiotropy의 다섯 가지 기본 모델 제안
모델 1: 유전자 수준의 변이가 여러 유전자에 영향을 미침
이 모델은 큰 유전자 삭제 또는 삽입과 같은 변이가 여러 유전자에 영향을 미치는 경우를 설명합니다. 이는 광범위한 유전적 변화를 초래하여 다양한 표현형에 영향을 미칠 수 있습니다.
모델 2: 단일 유전자의 다기능성
한 유전자가 대체 스플라이싱이나 엑손 스킵 같은 메커니즘을 통해 여러 기능을 가질 수 있습니다. 예를 들어, 하나의 유전자가 다양한 단백질 변형체를 생성하여 서로 다른 생물학적 과정에 관여할 수 있습니다.
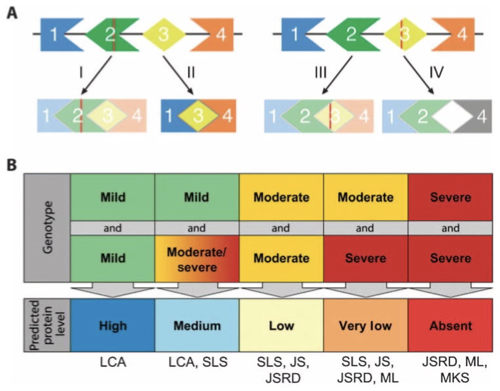
LCA (Leber Congenital Amaurosis):
LCA, 르베르 선천성 암맹증은 선천적이고 유전적인 망막 질환으로,
출생 시 또는 유아기에 심각한 시각 장애를 일으키는 것으로 알려져 있습니다.
LCA는 일반적으로 매우 심각한 형태의 망막 변성을 특징으로 하며, 망막 세포의 손상이나 사멸로 인해 진행됩니다.
JSRD (Joubert Syndrome-Related Disorders):
JSRD는 Joubert 증후군과 관련된 장애를 포괄하는 용어입니다.
이 질환들은 중추신경계(CNS)의 이상을 특징으로 하며,
특히 소뇌 벌집 및 뇌간의 발달 부진 및 근육 톤 저하가 관찰됩니다.
JSRD는 또한 신장 질환과 같은 추가적인 비중추신경계 증상을 포함할 수 있습니다.
ML (Meckel-like Syndrome):
Meckel-like 증후군은 Meckel-Gruber 증후군과 유사한 특징을 보이지만,
일반적으로 덜 치명적인 형태입니다.
이 증후군은 여러 기관의 중대한 관여로 인해 사망에 이르게 할 수 있습니다.
MKS (Meckel-Gruber Syndrome):
Meckel-Gruber 증후군은 치명적인 유전 질환으로,
신경관 결함, 다지증(많은 손가락 또는 발가락), 낭포성 신장 질환과 같은 심각한 다중 기관 관련 증상을 특징으로 합니다.
SLS (Senior-Løken Syndrome):
Senior-Løken 증후군은 망막과 신장 이상을 특징으로 하는 질환입니다.
이는 일반적으로 망막 변성과 함께 신장 기능 장애가 동반됩니다.
JS (Joubert Syndrome):
Joubert 증후군은 중추신경계, 특히 소뇌의 발달 이상이 특징입니다.
이는 조정 능력 저하, 저근력, 발달 지연 및 호흡 문제와 같은 증상을 동반할 수 있습니다.
모델 3: 유전자 제품의 다중 도메인 또는 조직 특이적 기능
유전자 제품(예: 단백질)이 여러 독립적인 기능을 가진 다중 도메인을 포함하거나, 다른 조직에서 다른 기능을 수행할 수 있습니다. 이는 단일 유전자 제품이 다양한 생물학적 역할을 수행할 수 있음을 의미합니다.
예: p53 단백질의 각 도메인은 고유한 구조적 특성과 접힘 패턴을 가지고 있으며, 이는 단백질이 다양한 기능을 수행. p53의 다기능성은 효소활성 및 DNA 결합활성을 갖는다.
예: 섬유아세포 성장 인자(FGF)는 다양한 조직에서 다른 기능을 수행합니다. 예를 들어, FGF는 피부 조직에서는 상처 치유와 세포 재생을 촉진하는 반면, 뇌에서는 신경 세포의 성장과 발달을 돕습니다. 이러한 기능의 다양성은 FGF가 조직에 따라 다른 리셉터와 상호 작용하거나 다른 세포 신호 경로를 활성화하기 때문에 가능합니다.
모델 4: 단일 기능이 여러 표현형에 영향
한 유전자 제품이 하나의 기능을 가지고 있지만, 즉 여러 조직에서 같은 기능을 수행하지만 그 영향이 각기 다른 조직에서 다르게 나타나는 현상을 의미
예: 마르판 증후군은 FBN1 유전자의 돌연변이가 여러 기관의 결합 조직에 영향을 미쳐 골격, 안구, 피부 및 심혈관 증상을 유발하는 질환
모델 5: 하나의 특성이 다른 표현형을 유발
하나의 복잡한 질병 또는 특성이 생리적 변화를 통해 다른 표현형의 출현을 유발할 수 있습니다.
예: SERPINA1 유전자의 돌연변이는 α1 항트립신 결핍을 유발하며, 이 장애는 폐 염증을 유발하여 폐기종을 유발하여 COPD63의 위험을 증가시킵니다.
예: 거의 모든 제1형 당뇨병(T1D) 환자는 고혈당증에 의해 유발되는 병리 생리학적 메커니즘으로 인해 당뇨병성 망막병증이 발병
*모델5를 제외한 모든 모델은 맥락상 ‘true’ pleiotropy로 간주
*두 질병이 공유된 유전적 요인(모델 1과 2), 공유된 질병 경로(모델 3과 4)
Difficulties in defining a phenotype
: ‘true’ pleiotropy 이란 무엇인가
연구 중인 시스템과 특성에 따라 달라진다.
1. 개인 수준에서 유전적 변이가 여러 질병과 관련이 있을 때 이를 다형성으로 간주하는 경우
2. 같은 세포 내에서 여러 표현형에 기여할 때만 이 변이를 다형성으로 간주
Pleiotropy and its role in comorbidities.
모델5의 경우, 첫 번째 질병을 치료하는 것이 두 번째 질병의 발생을 예방할 수 있습니다.
예: 적절한 혈당 조절은 제2형 당뇨병(T2D)의 공존 질병인 당뇨병성 망막병증의 발생을 막을 수 있다.
모델1-4의 경우, primary disease를 치료한다고해서 나머지 질병을 예방할 수 있다는 것은 아니다.
따라서 동시 발생을 모델 중 하나로 설명할 수 있는지 여부를 밝히는 것이 중요해보지만,
일반적으로 모델이 혼합된 형태로 나타낸다. 그리고 모델1-4를 구분하하는 것은 불가능하다(구체적인 분자 메커니즘을 알아야한다.)
마지막으로, 공유 유전자 또는 경로는 두 질병의 원인이 어떻게 겹치는지를 정확히 이해하는데 유용하다.
*PheWAS는 건강 기록에서 상세한 임상 데이터와 연동된 유전자형 데이터를 결합하여 유전자형-형질 연관을 감지할 수 있으며, 이는 복수형 연관을 식별하고 신약 재활용 후보를 제안하는 데 큰 약속을 품고 있습니다(65,66)
예: 항레트로 바이러스 약인 zidovudine(지도부딘)은 HIV 및 에이즈 치료에 사용되는데, 이것이 당뇨병 치료를 위해 재활용되었습니다.
Methods for studying pleiotropy and multifunctionality.
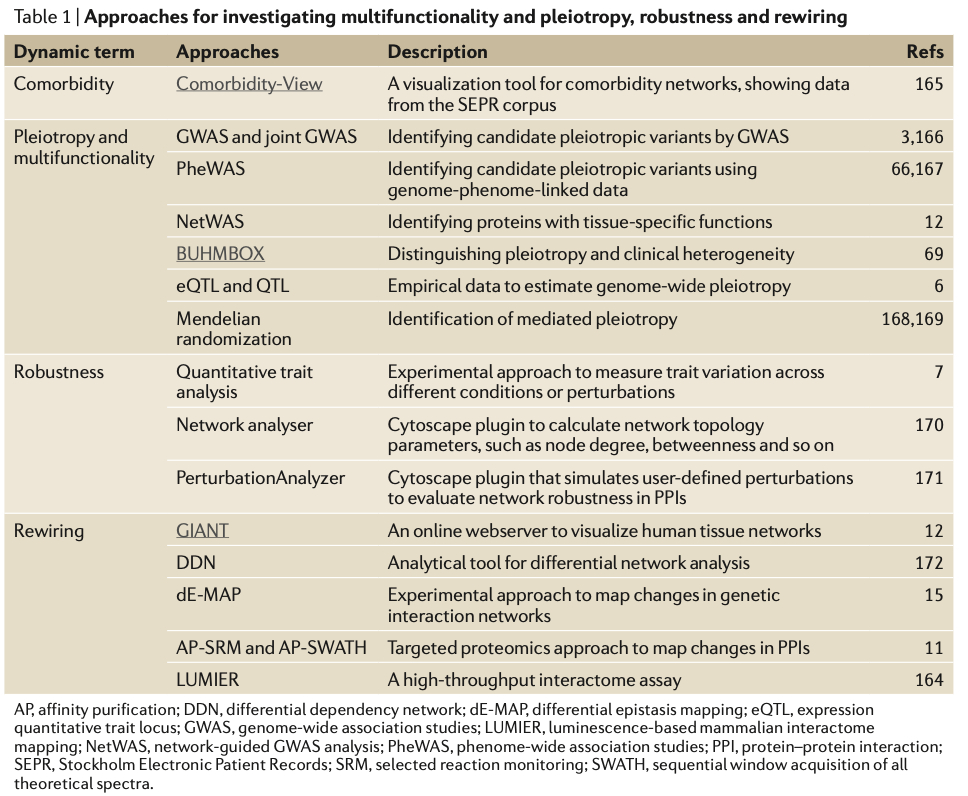
1. 다중 기능성을 식별하기 위한 적절한 분석 전략들이 개발되었습니다.(Table 1)
2. GWAS를 통해 질병들을 함께 연구하면 단일 질병 연구에서 찾을 수 없는 다중 기능성 위험 변이를 발견할 수 있습니다.
*대부분의 PheWAS 및 GWAS는 단일 질병에만 국한되지 않고 여러 질병 및 형질과의 연관성을 검사할 수 있기 때문에 다중 기능성 효과를 발견하는 데 유용하다.
5. BUHMBOX, 다중 기능성과 이질성을 구별하기 위한 온라인 도구
*heterogeneity : 한 질병의 일부 케이스만이 다른 질병과 유전적으로 동일한 경우를 나타내는 경우
*pleiotropy : 둘 이상의 질병 간의 동반 질환
*최근에는 다섯 가지 만성 염증성 질환 간의 관계를 분석하여 다중 기능성을 밝혀내고, 단일 질병 연구만 사용했을 때 놓칠 수 있는 공유 위험 지역을 식별
Robustness
Defining robustness.
1. (생물학적 시스템의 특징) : 시스템이 내부 및 외부 변동에 대항하여 기능을 유지하는 속성
그리고 규모가 없는 네트워크 아키텍처와 특성들은 이런 변동에 네트워크의 기능성을 유지한다.
2. (개체의 표혀형의 특징)
주요 문제
1. homeostasis(홈오스태시스)과 같은 관련 개념과 명확하게 구분되지 않은 경우
*homeostasis : The ability to sustain various physiological parameters in a steady state.
2. 어떻게 측정되는지 및 고려된 변동의 성격이 무엇인지를 명확히 명시하지 않은 채 일반적으로 사용
Robustness of a system.
생물학적 시스템이 변동에 노출될 때, 그것은 그 변동에 대해 로버스트하게 유지되어 기능성(예: 표현형)을 유지할 수도 있고 기능성이 변경될 수도 있습니다. 유지하더라도 내부 물리상태는 변경될 수 있으므로 다른 변동에 취약해질 수 있다.
예를 들어, 신체의 생리적 역학은 불안정한 식량 공급과 병원균 감염에 대한 로버스트성을 보장하기 위해 진화해 왔지만, 동시에 이러한 역학은 과다 영양과 같은 환경 변화에 취약할 수 있으며 이로 인해 대사 증후군과 같은 복잡한 질환으로 이어질 수 있습니다.
Phenotypic robustness and missing heritability.
* GWAS는 유전적 변이가 형질적 변이와 어떻게 관련되는지를 부분적으로만 설명할 수 있었으며(‘빠진 유전성’ 개념을 도출함), 드문 돌연변이, 약한 영향을 미치는 변이 및 상호작용과 같은 다른 요인들도 중요한 역할을 한다는 것을 시사합니다.
*잠재적인 질병 원인 변이는 형질적으로 로버스트한 개체에서는 숨겨질 수 있지만, 덜 로버스트한 개체에서는 영향을 줄 수 있으며, 이러한 변이는 감지하기 어려울 수 있습니다.
예: 589,306 개의 유전체 분석에서 13 명의 성인은 심각한 멘델병적 상황을 가진 돌연변이를 가지고 있었지만 질병의 발현증세가 없었습니다.
일부 개인의 보호적 변이가 동반변동의 가능성을 증가시키는 변동에도 불구하고 다병질 공간에서 그들을 동일한 상태로 유지할 것이라는 것을 시사
Readouts of phenotypic robustness.
*로버스트성이 낮은 개체들은 여러 복잡한 질병에 더 높은 위험을 갖음
*로버스트성에 기여하는 원천들 : 보호적 변이 등
예: 몇 가지 CNV는 멘델병이나 복합성 질병 변이로서 질병 감수성과 관련이 있다고 합니다. 그러나 정신분열증, 자폐증, 간질, 당뇨병 및 지적 장애 등 여러 복합 질병에서 관찰된 드문 CNV들은 통제 인구에서도 발견됩니다. 이러한 CNV들은 반드시 질병에 특이적이지 않기 때문에 일부 개체들에서의 형질적 로버스트성의 감소의 결과일 수 있습니91 92
Rewiring
종종 '변화'의 동의어로 일반적으로 사용
Defining rewiring.
1. 생물학적 시스템이 "다양한 조건"에 따라 "상호작용을 다시 구성함"을 나타낸다.
*예를 들어, 영양 공급의 변화나 세포 분열과 같은 생물학적 프로세스는 생물학적 네트워크의 재배선을 유발할 수 있습니다.
*이때 재배선은 네트워크 상에서 유전자나 단백질 간의 상호작용이 바뀌는 것을 의미합니다.
*생물학적 시스템이 외부 조건에 적응하기 위해 상호작용을 다시 구성하는 것이기 때문에 재배선은 자연스러운 현상
2. 주로 유전자나 단백질 상호작용을 매핑하여 측정
예: 암세포의 재배선을 연구할 때는 세포 내에서 발생하는 단백질 상호작용의 변화를 관찰하는 것이 중요
3. 재배선은 생물학적 시스템의 로버스트성에도 영향을 줍니다
*적응적 재배선은 시스템이 다양한 조건에 대해 안정된 상태를 유지
*변이적 재배선은 시스템을 질병 상태로 이끔
:로버스트성에 영향을 준다는 것은, 시스템이 외부 변화에 대해 얼마나 잘 견고하게 유지되는지에 영향을 미친다는 의미입니다. 생물학적 시스템은 외부에서 발생하는 변화에 대응하기 위해 자신의 구조를 조정하거나 재배선합니다. 이 재배선 과정은 시스템이 변화에 민감하게 반응하는지, 아니면 안정되게 유지되는지를 결정합니다. 따라서 재배선은 시스템의 로버스트성을 결정하는 중요한 요소 중 하나입니다.
4. 네트워크 기반 질병 유발 유전자와 생물학적 표지자를 발견 및 우언순위 지정에 사용 100
-> 동적 상호작용을 이해함으로써 효과적인 치료 전략 개발 가능
Rewiring in context.
*시간적 척도와 조건과 같은 맥락 안에서만 적절하게 해석이 가능하다
예: 80,000개의 유전자 상호작용을 두 가지 조건에서 테스트할 때 70% 이상의 양의 유전자 상호작용이 다른 것을 발견
*서로 다른 유형의 생물학적 네트워크는 서로 다른 속도로 재배선될 수 있다.
예: 전사 조절 상호작용은 단백질 상호작용보다 빠르게 재배선될 수 있다.
* 어떤 유형의 재배선 분석이 고려되는지를 강조하는 것이 중요
예:
하나의 시스템 내에서 상태를 비교할 수도 있고(예: 건강한 상태 대 질병 상태)
다른 시스템 간에 비교할 수도 있기 때문(예: 다른 조직 유형에서 단백질의 상호작용 파트너)
(요약)Rewiring을 고려한 동적 네트워크를 구성할 때는 시간적 척도와 조건이 같아야 하며, 서로 다른 유형의 생물학적 네트워크는 서로 다른 속도로 rewiring될 수 있습니다. 또한, 하나의 시스템 내에서의 rewiring과 다른 시스템 간의 rewiring을 구분하여 분석해야 합니다.
Rewiring of multifunctional proteins.
*단백질의 재배선 결과는 네트워크 내 위치에 따라 다르다. (왜? 모델3과 같이 다기능성을 갖기 때문)
->다른 환경 또는 유전적 조건에서 다른 기능을 취할 수 있습니다.
->또한, 상호작용 파트너의 풍부도 변화는 경쟁 상호작용을 통해 다기능성 단백질의 재배선에 영향을 미치며,
이를 통해 다양한 복합체나 경로에서의 참여를 규정합니다.
figure4. a
동적 VS 차이 네트워크
*동적 네트워크는 시간을 통해 지속적으로 재배선되는 여러 네트워크 상태
*차이 네트워크는 두 정적 네트워크 상태 간의 변화를 식별
-> 차이 네트워크는 두 측정 조건 간의 모든 상태 변화를 감지하지 못할 수 있다.
figure4.b
*이러한 상호작용 파트너의 풍부도가 감소하면 대안 상호작용 파트너(blue)에 결합이 우선
*상호작용 파트너의 풍부도 변화에 따라 비선형 스위치와 유사한 메커니즘을 통해 재배선이 발생
Dynamic elements as network bottlenecks
*재배선, 로버스트성 및 플레이오토로피에 관한 연구에서 중심 네트워크 위치의 단백질이 질병 발생에서 중요성을 강조해왔다.
-> hub protein = proteins at central network position = important -> might be pleiotropic genes
예: 염증성 질환의 연구에서 중심 단백질이 다른 질병 상태에서 겹치는 경로를 재배선함
*생물학적 네트워크는 종종 무작위한 변동에 대해 견고하지만, 허브나 병목 노드와 같은 중심 노드를 타격하는 변동에 대해 취약하다.
*허브 유전자의 재배선은 많은 엣지의 동시적인 재배선으로 이어질 수 있지만, 반드시 다른 세포 과정으로 이어지지는 않는 반면
*병목 유전자의 재배선은 여러 과정에 영향을 미칠 수 있다.
*hub : 많은 다른 노드와 연결된 노드
*bottelneck : 서로 다른 subnetwork를 잇는, betweenness가 높은 노드
*병목 단백질은 네트워크에서 주요 연결자이므로 세포가 상태 전환을 위해 사용하는 주요 재배선 전환 지점일 수 있다.
box1
*network : 노드(단백질, 유전자, 질병 등) + 엣지(기능적 혹은 물리적 관계) 예: PPI 물리 상호 네트워크, 질병간의 원인과 결과 관계 네트워크 등
*노드 차수(node degree)(k)는 노드에 연결된 엣지의 수
*P(k) 는 네트워크의 각 노드들이 갖는 엣지의 개수에 대한 분포
*두 노드 사이의 최단 경로는 그들을 연결하는 최소한의 엣지 수
*평균 경로 길이는 모든 노드 쌍 간의 평균 최단 경로이며, 네트워크의 탐색 가능성을 측정하는 지표
*매개 중심성(betweenness centrality)은 네트워크에서 얼마나 중심적인지를 나타내는 측정 지표
-> 매개 중심성이 높은 노드를 제거하면 평균 경로 길이가 증가할 것이다.
Scale-free versus random networks
- Scale-free network (절대비례 네트워크):
- Scale-free network는 노드의 연결 수가 일정한 분포를 따르지 않고, 일부 노드는 매우 많은 연결을 가지고 있으며(허브), 대다수의 노드는 소수의 연결을 가지고 있는 특징을 갖는 네트워크입니다.
- 이러한 네트워크는 일부 노드가 많은 연결을 가지기 때문에 공격에 대해 견고하며, 랜덤한 장애에 대해서는 보다 견고하게 동작합니다.
- 대부분의 생물학적 네트워크(단백질 상호작용 네트워크, 대사 네트워크 등)와 인터넷과 같은 실제 세계의 네트워크는 일반적으로 scale-free 특성을 갖습니다.
- Random network (랜덤 네트워크):
- Random network는 노드 간의 연결이 완전히 랜덤하게 형성되는 네트워크입니다. 이것은 모든 노드가 거의 동일한 수의 연결을 가지며, 연결의 분포가 포아송 분포를 따르는 특징을 가집니다.
- 이러한 네트워크는 특정한 노드들이 매우 높은 중심성을 갖지 않기 때문에, 특정 노드의 손상이 전체 네트워크에 큰 영향을 미치지 않습니다.
- 예를 들어, 간단한 무작위 네트워크는 인터넷에서 단일 컴퓨터의 고장이 인터넷의 전체적인 동작에 큰 영향을 미치지 않는 이유를 설명하는 데 사용될 수 있습니다.
모듈성(Modularity):
- 모듈성은 네트워크에서 서로 밀접하게 연결된 그룹(또는 모듈)들의 밀도를 나타내는 지표입니다. 이는 네트워크가 여러 모듈로 나뉘어져 있고, 모듈 내의 노드들이 서로 밀접하게 연결되어 있을 때 높은 값을 갖습니다.
- 모듈성은 -1에서 1 사이의 값을 가지며, 값이 양수일수록 네트워크의 모듈 구조가 강조됩니다.
보우타이(Bow tie):
- 보우타이는 네트워크의 멀티레이어 구조를 설명하는 개념입니다. 이는 네트워크가 입력 및 출력 레이어, 코어 컴포넌트, 그리고 보조 컴포넌트로 나뉘는 구조를 가질 때 적용됩니다.
- 보우타이 구조는 다음과 같은 요소로 구성됩니다:
- 입력 레이어(Input layer): 네트워크의 입력 노드들로 구성되며, 외부로부터의 입력을 받습니다.
- 코어 컴포넌트(Core component): 입력 및 출력 레이어 간의 연결된 중요한 노드들의 집합으로, 네트워크의 핵심 부분을 형성합니다.
- 출력 레이어(Output layer): 네트워크의 결과를 출력하는 노드들로 구성되며, 외부로 결과를 전달합니다.
- 보조 컴포넌트(Auxiliary component): 코어 컴포넌트와 입력 또는 출력 레이어 사이의 중간 단계에 있는 노드들로 구성되며, 보조적인 역할을 수행합니다.
- 보우타이 구조를 분석하는 방법은 네트워크의 레이어 및 컴포넌트를 식별하고, 각 구성 요소의 상호작용 및 영향력을 평가하는 것입니다.
hubs and bottlenecks
허브 노드는 네트워크 내에서 많은 다른 노드와 상호작용하며, 따라서 종종 중심 위치를 차지합니다.
반면에, 병목 노드는 많은 상호작용을 갖지 않을 수 있지만 betweenness centrality가 높습니다.
*이는 병목 노드가 종종 서로 다른 하위 네트워크 간의 연결자 역할을 하게 됨을 의미합니다.
노드는 허브와 병목 둘 다 될 수 있습니다.
병목 노드를 제거하면 허브 노드를 제거하는 것보다 네트워크의 분리가 더 많이 발생할 가능성이 높습니다.
Redundancy and degeneracy
중복 및 탈성은 시스템 내의 견고성을 유지하는 데 기여
*중복이란, 예를 들어 두 노드가 여러 경로로 연결된 경우를 말합니다. 하나의 경로가 제거되어도 노드들은 여전히 연결됩니다.
*탈성은 겹치는 및 분리된 효과를 동시에 나타내는 고유한 중복의 유형입니다.
(즉 두 노드가 여러 경로로 연결되어있어, 분리되면서도 겹치는 효과를 누릴 수 있다. 예: 이것은 각 노드 또는 구성 요소가 개별적으로 작동할 때 서로 다른 결과를 내면서도 특정 기능 또는 목표를 달성하는 데 도움이 되는 겹치는 효과를 가져옵니다. )
Box 2 | Mapping network changes
네트워크 재배선을 분석하는 주요 전략과 기술은 세 가지입니다.
첫 번째는 통합적인 '정적-시간적 접근 방법
이 방법은 정적 네트워크 데이터와 다양한 조건 또는 시간 지점의 고처리량 분자 프로필(예: 유전자 발현)을 겹쳐 분석합니다. 이 접근 방법은 조건별 정적 상호작용을 추출할 수 있지만, 원래의 정적 상호작용에만 의존하므로 새로운 동적 상호작용을 감지할 수 없는 한계가 있습니다.159-161
두 번째 방법은 최근에 나온 '차별 네트워크 매핑 접근 방법'
이 방법은 다른 조건에서 네트워크를 생성한 다음 변경된 조건에 가장 영향을 받는 부분을 강조하기 위해 네트워크를 빼는 방식입니다. 유전 상호작용을 기반으로 한 이 방법은 유전자와 관련된 단백질이 참여하는 경로 사이의 기능적 관계를 반영합니다. 차별 에피스타시스 매핑(dE-MAP)은 특정 응답에 특화된 상호작용을 드러내고 일반적인 상호작용을 필터링합니다. 그러나 고등 생물에서는 실험적 상호작용을 조사해야 하므로 이 방법은 비용과 노동 집약적입니다.
세 번째는 차별적 공동발현 네트워크인데, 이는 유전자 발현 데이터를 사용하여 질병과 대조군 샘플의 공동발현 네트워크를 비교합니다. 물리적 단백질-단백질 상호작용의 경우 목표 지향적 단백질체학 기법을 사용하여 다양한 시간 지점과 조건에서 동적 상호작용을 조사할 수 있습니다. 162
마지막으로, 야광기반 포유류 상호작용 매핑(LUMIER) 164
이는 루시페라제-융합 '먹이' 단백질과 '사냥감' 단백질 간의 이진 상호작용을 다양한 조건에서 측정할 수 있는 기술입니다. 이 기술은 뇌 세포에서 조직 특이적 재배선을 연구하는 데 사용되었으며, 엑손 종속적 효과를 연구하기 위해 먹이 단백질을 특정 엑손으로 변경하는 등 다양한 응용이 가능합니다.
- Bait(먹이): 연구자가 관심을 가지는 단백질로, 상호작용을 조사하고자 하는 주체입니다. 이 단백질은 다른 단백질과 상호작용을 하기 위해 특정 실험적 조건 하에서 변형되거나 표현될 수 있습니다.
- Prey(사냥감): 먹이 단백질과 상호작용하는 다른 단백질로, 실험에서 먹이 단백질과 상호작용하는 후보 단백질입니다. Prey는 먹이 단백질과의 상호작용을 탐지하기 위해 특별히 디자인된 실험 조건에서 표현됩니다.
Dynamics of immune-mediated disease
면역 매개 질환의 동역학
- 단일 질환 관점 또는 개념적 측면에서 질병을 분석하는 것은 여러 수준의 질병 동역학을 무시합니다.
- 합병증을 조사하기 위한 시스템 생물학 접근법이 나타나면서 세 가지 네트워크 개념을 통합하는 실생활 예시가 아직 없습니다.
- 면역 매개 질환은 많은 공유 질병 위험 변이와 다양한 분자 및 세포 형질을 가지고 있으며, 이를 함께 분석하는 것이 질병 동역학의 완전한 그림을 얻는 데 유용할 수 있습니다.
- 면역 매개 질환은 각 질환 유형 내에서도 매우 다양한 형질을 보이며, 그 원인은 완전히 알려지지 않았습니다.
- 면역 매개 질환은 호스트 자체를 공격하는 면역 체계의 기작이 잘못되는 결과로 발생한다고 여겨지며, 이는 자기 반응성 세포를 걸러내는 데 중요한 변형 티뮴 선택과 관련이 있습니다.
- 질병 발병은 질병 전 발병이 확립된 후 몇 년 후에 발생할 수 있어 질병의 원인을 명확히 하는 것이 어렵습니다. 그러나 면역 매개 질환의 일부 환경적 유도 요인은 도식화됩니다.
- 면역 매개 질환은 질병 위험 변이와 경로의 광범위한 중첩을 보여주며, 이는 플레이오토피 효과의 제안적인 효과를 나타냅니다.
- 면역 매개 질환의 환경 요인은 여전히 시간이 경과함에 따라 질병의 발현을 유도하여 개인이 새로운 위치로 전환되도록 할 수 있습니다.
예: 저염성 상태의 임상 동반성이 중첩된 병태생리적 경로와 관련이 있으며, 해당 환자가 관련 증후군을 가진 환자와 유전적으로 다르다는 결론을 내렸습니다.
예: 중복 질병의 최소한 일부가 경로 수준에서 나타나는 공통 위험 변이를 가진다는 것을 보여주었습니다.
예: 플레이오토피 변이는 주요 조직 적합성 복합체(MHC)와 관련된 과정에 관여하며, 희귀 변이와 결합하여 환자의 특정 질병 형질을 결정
*여러 CNV와 단일 염기 다형성이 면역 매개 질환과 관련되어 있으며, 면역 관련 유전자는 이러한 변이로 풍부
도전:
1. 다중 수준의 질병 역학을 분석하기 위한 시스템 생물학적 접근 방식의 부족.
2. 다양한 질병의 복잡한 동적 변화를 이해하기 위한 데이터 부족.
3. 인구 수준의 건강 데이터의 급격한 증가로 인한 데이터 처리 및 해석의 어려움.
4. 새로운 분자 수준 데이터 유형의 시스템적 생성과 분석을 위한 인프라 부족.
5. 환자의 개별적인 유전자 변이 및 생리학적 특성을 고려한 정확한 진단 및 치료의 어려움.
전망:
1. 정밀 의학 프로젝트의 진행과 함께 전자 건강 데이터 및 분자 수준 데이터의 통합적 수집 및 분석.
2. 임상 단백체학 및 메타볼로믹스 기술의 발전으로 인한 동적 분자 수준 데이터의 시스템적 생성 및 해석.
3. 더 많은 건강 상태 데이터 및 시간에 따른 데이터의 사용으로 질병 전환 및 진행에 대한 이해 향상.
4. 분자 네트워크 생물학 수준에서 동적 모델의 발전과 활용을 통한 정확한 진단 및 개인 맞춤형 치료 전략의 개발.
5. 건강 데이터의 대규모 연구를 통해 다중 질병과의 상호 작용 및 관련성에 대한 더 나은 이해와 치료 방법의 개발.
Methods
소제목입니다.
method의 원리 및 수식을 이해하고 정리합니다.
(이해를 바탕으로 작성합니다.)
Results
결과를 요약하고, 그 결과가 시사하는 바를 정리합니다.
(결과를 비판적으로 생각하며 작성합니다.)
Conclusions
장,단점을 정리합니다.
(자신의 연구와 어떻게 접목시킬지 생각하며 작성합니다.)



